El neumotórax se define como la presencia de aire o gas en el espacio pleural. Este espacio virtual está
situado entre la pleura visceral, que recubre el parénquima pulmonar externamente, y la pleura
parietal, que recubre la fascia endotorácica, el mediastino y el diafragma.
Se denomina neumotórax espontáneo (NE) cuando ocurre sin ninguna causa desencadenante,
como traumatismo o procedimiento quirúrgico o diagnóstico invasivo. Es una enfermedad torácica
frecuente; se estima que la tasa de ingresos anual es de 16,7/100.000 para los hombres y 5,8/100.000
para las mujeres. En contra de la creencia generalizada que los relaciona con el esfuerzo, el 90% de
los NE tienen lugar en reposo.
En función de la ausencia o presencia de enfermedad pulmonar previa, el NE se clasifica en
primario y secundario, respectiv amente. El primario tiene su máxima incidencia entre los 20 y los 30
años, mientras que el secundario tiene su pico de incidencia por encima de los60 años, debido a su
asociación con la enfermedad pulmonar obstructiva crónica (EPOC) (26/100.000 enfermos).
ETIOLOGÍA
Neumotórax espontáneo primario
En el 90% de los pacientes se origina por la rotura de blebs o bullas, que son quistes aéreos
subpleurales menores o mayores de 2 cm, respectivamente. Entre los factores etiológicos que se
relacionan con el desarrollo y la rotura de estas lesiones están el tabaco (el 90% de los pacientes
afectados son fumadores), la predisposición genética (asociación familiar en el 10% de los casos), la
talla alta (hábito leptosomático), el sexo (proporción hombre: mujer de 2,5:1), la edad (tercera década
de la vida) y los cambios en la presión atmosférica.
Neumotórax espontáneo secundario
Su etiología es multifactorial y está condicionada por la enfermedad pulmonar de base (tabla 42.1).
Así, en la EPOC, el neumotórax se debe a la rotura de bullas, mientras que en pacientes con sida y
neumonía por Pneumocystis jiroveci, se debe a necrosis pulmonar.
Tabla 42.1 Causas de neumótorax espontáneo secundario
ENFERMEDADES DE LA VÍA AÉREA
Enfermedad pulmonar obstructiva crónica (EPOC)
Fibrosis quística
Asma
ENFERMEDAD PULMONAR INTERSTICIAL DIFUSA
Fibrosis pulmonar idiopática
Sarcoidosis
Histiocitosis X
Linfangioleiomiomatosis
INFECCIONES PULMONARES
Neumonía por Pneumocystis jiroveci
Tuberculosis
Neumonía necrotizante
Hidatidosis
ENFERMEDADES DEL TEJIDO CONECTIVO
Artritis reumatoide
Espondilitis anquilopoyética
Polimiositis/dermatomiositis
Esclerodermia
Síndrome de Marfan
Síndrome de Ehlers-Danlos
NEOPLASIAS
Cáncer broncogénico
Metástasis pulmonares de sarcoma
OTRAS
Esclerosis tuberosa
Neumoconiosis (silicoproteinosis, beriliosis, bauxita)
Granulomatosis de Wegener
Drogas y toxinas (crack, paraquat, pentamidina en aerosoles)
Quimioterapia
Radioterapia
Oxígeno hiperbárico
Infarto pulmonar
Neumotórax catamenial
Suele considerarse un caso especial de NE. Se presenta en el 3–6% de las mujeres en edad fértil, más
frecuentemente entre los 20 y los 40 años de edad, y generalmente durante las 72 h siguientes al inicio
de la menstruación. En el 90% de los casos se localiza en el hemitórax derecho.
FISIOPATOLOGÍA Y CLÍNICA
La salida de aire desde el parénquima pulmonar, a través de una disrupción en la pleura visceral,
provoca que la presión intrapleural se aproxime a la atmosférica y se origine colapso pulmonar, con
separación de ambas hojas pleurales. El grado de colapso depende de varios factores, como la
capacidad de retracción elástica del pulmón, aspecto relevante en el NE secundario, en el que suele
estar disminuida y pequeños colapsos pueden originar grandes alteraciones funcionales.
La alteración más importante es una disminución de la presión arterial de oxígeno (PaO2) y un
aumento de la diferencia alveoloarterial (ΔAaPO2). Dependiendo del grado de colapso pulmonar y de
la reserva funcional del paciente, las alteraciones gasométricas pueden variar desde alcalosis
respiratoria por hiperventilación hasta acidosis respiratoria con hipercapnia.
En general, el NE primario en sujetos jóvenes y sanos es bien tolerado, con mínimos cambios en
los signos vitales; por el contrario, el NE secundario, al ocurrir en pacientes mayores con
comorbilidad asociada, puede originar insuficiencia respiratoria grave e inestabilidad cardiovascular,
aunque sea pequeño.
Los síntomas más frecuentes (90% de los episodios) son el dolor torácico de características
pleuríticas y la disnea, ambos de aparición brusca e intensa. El signo clínico más constante es la
disminución del murmullo vesicular a la auscultación en el hemitórax afectado. En el 1–3% de los
pacientes pueden detectarse complicaciones, como neumotórax a tensión, neumotórax bilateral
simultáneo y hemoneumotórax espontáneo.
El neumotórax a tensión (fig. 42.1) se define como todo neumotórax, independientemente de su
tamaño, que provoca desviación contralateral del mediastino, colapso cardiovascular e insuficiencia
respiratoria grave con hipoxia tisular. La presión intrapleural es superior a la atmosférica. Todos los
síntomas y signos del neumotórax son más prominentes: disminución de la ventilación y de los
movimientos respiratorios, hiperresonancia a la percusión, desviación traqueal contralateral,
ingurgitación yugular, taquicardia, taquipnea e hipotensión arterial.
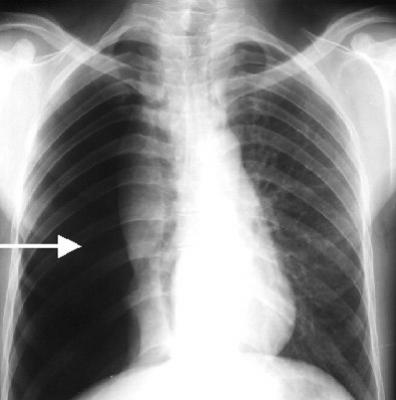
Figura 42.1 El tamaño del neumotórax debe clasificarse según la acumulación de aire visible en la radiografía posteroanterior, es
decir, la distancia entre la «línea pleural» y el borde interno de la pared torácica (A-B).
E l hemoneumotórax espontáneo se origina por la rotura, durante el colapso pulmonar, de
adherencias pleuropulmonares vascularizadas. Según su magnitud puede ser necesario tratamiento
quirúrgico urgente (toracotomía o videotoracoscopia).
EXPLORACIONES COMPLEMENTARIAS
Radiografía de tórax
Cualquier neumotórax clínicamente significativo debe visualizarse en una radiografía de tórax,
tanto en proyección posteroanterior como lateral; no obstante, en caso de duda diagnóstica, puede
recurrirse a una proyección posteroanterior en espiración forzada, o a una proyección en decúbito
lateral contralateral (hemitórax afectado elevado) con rayo horizontal.
Los signos radiológicos principales son la existencia de una «línea pleural», debida al aumento de
densidad de la pleura visceral en el pulmón colapsado, que dibuja su contorno, una diferencia de
densidad entre el pulmón colapsado (densidad agua) y la cavidad pleural (densidad aire), y una
interrupción de la vascularización pulmonar, a nivel de la línea pleural, que se extiende radialmente
desde el hilio pulmonar hacia dicha línea. Esta línea pleural nunca excede los límites de la cavidad
intratorácica, y pueden confundirse con ella imágenes originadas por el borde interno de la escápula,
pliegues cutáneos en sujetos obesos, pliegues de la ropa, sondas de oxigenoterapia y,
fundamentalmente, bullas de enfisema.
La existencia de un nivel hidroaéreo o un borramiento del hemidiafragma (500 ml de líquido,
aproximadamente) debe alertar de la existencia de un hemoneumotórax espontáneo.
Según las indicaciones de la British Thoracic Society, el tamaño del neumotórax debe clasificarse
según el grado de acumulación de aire visible en la radiografía posteroanterior de tórax, entre la «línea
pleural» y el borde interno de la pared torácica (v. fig. 42.1). De esta forma el neumotórax es:
• Pequeño, si esta distancia (A – B) es inferior a 2 cm.
• Grande, si la distancia (A – B) es igual o mayor a 2 cm.
El volumen que ocupa un neumotórax se calcula según la siguiente fórmula:
Así, un neumotórax de 1 cm (pequeño) ocupa un volumen aproximado del 27% del hemitórax en
la radiografía de tórax en proyección posteroanterior, mientras que un neumotórax radiográfico de 2
cm (grande) ocupa el 49%.
Tomografía computarizada torácica
Únicamente está indicada si hay duda diagnóstica, especialmente en el diagnóstico diferencial con
bulla enfisematosa, en aquellos casos en los que el propio enfisema pueda ocultar la existencia de un
neumotórax sospechado clínicamente o ante la posibilidad de una herniación intratorácica gástrica
(muy infrecuente). En ocasiones está indicada para la cuantificación de un hemoneumotórax
espontáneo.
Otras pruebas complementarias
No son imprescindibles para el diagnóstico y el tratamiento del neumotórax; no obstante, es
aconsejable su realización por la información adicional que aportan, especialmente si está indicada la
intervención quirúrgica.
Saturación arterial de oxígeno (SaO2) si hay disnea o dificultad respiratoria. Debe mantenerse por
encima del 92%.
Gasometría arterial. Sólo está indicada en pacientes con patología pulmonar de base o si se
sospecha retención de CO2.
Hematimetría con fórmula y recuento leucocitarios, para valorar la existencia de una anemia
aguda sugestiva de hemoneumotórax.
Bioquímica sanguínea que incluya la determinación de glucosa, urea, creatinina e iones.
Estudio de coagulación.
Electrocardiograma.
CRITERIOS DE INGRESO
Todos los pacientes con NE diagnosticado requieren ingreso hospitalario.
TRATAMIENTO
Medidas generales
Reposo en cama con la cabecera elevada.
Canalización de una vía venosa periférica, preferiblemente con Drum, para la medición de la
presión venosa central, y perfusión de suero fisiológico a un ritmo inicial de 21 gotas por minuto.
Monitorización continua del ritmo y de la frecuencia cardíacos, frecuencia respiratoria, presión
arterial y SaO2 mediante pulsioximetría.
Administración de oxígeno mediante mascarilla tipo Venturi (Ventimask®) a una concentración
superior al 28%, para mantener la SaO2 por encima del 92%, por lo menos, hasta el tratamiento
definitivo, excepto que exista contraindicación expresa (hipercapnia crónica). Esta medida, además de
mejorar la oxigenación tisular, aumenta la capacidad de reabsorción pleural del neumotórax.
Analgésicos, como paracetamol (Perfalgan®, viales de 100 ml con 1 g) por vía intravenosa, en
dosis de 1 g/6 h, perfundido en 15 min; o metamizol magnésico (Nolotil®, ampollas con 2 g), en dosis
de 2 g/6 h por vía intravenosa; para ello se diluye una ampolla del preparado comercial en 100 ml de
suero fisiológico o glucosado al 5%, y se perfunde en 20 min. Si el dolor no cede, puede añadirse
tramadol (Adolonta®, ampollas con 100 mg), en dosis de 100 mg/8 h por vía intravenosa. En
ocasiones es necesaria la administración de morfina (Morfina Braun®, ampollas de 1 ml con 10 mg y
de 2 ml con 40 mg), en dosis de 2 mg/min por vía intravenosa, hasta que desaparezca el dolor o hasta
llegar a una dosis máxima total de 10 mg. Si una vez transcurridos 10 min el paciente continúa con
dolor, se repite la dosis mencionada. Para administrar este fármaco, a la presentación comercial de
morfina de 10 mg deben añadirse 9 ml de suero fisiológico, y perfundir a razón de 2 ml/min (1 ml
equivale a 1 mg).
Si no existe hemoneumotórax, está indicado tratamiento anticoagulante profiláctico con heparinas
de bajo peso molecular, como una de las siguientes:
• Bemiparina (Hibor®, jeringas precargadas de 0,2, 0,2, 0,2, 0,3 y 0,4 ml con 2.500, 3.500,
5.000, 7.500 y 10.000 UI, respectivamente), en dosis de 3.500 UI/24 h, por vía subcutánea.
• Enoxaparina (Clexane®, jeringas precargadas de 0,2, 0,4, 0,6, 0,8 y 1 ml con 20, 40, 60, 80 y
100 mg, respectivamente; Clexane Forte®, jeringas precargadas con 90, 120 y 150 mg), en dosis
de 1 mg (100 UI)/kg/24 h, por vía subcutánea.
Debe recomendarse la abstención tabáquica.
Tratamiento específico
Si se trata de un NE primario apical, con una distancia del vértice pulmonar a la cúpula pleural
inferior a 3 cm, en pacientes asintomáticos, se realiza tratamiento conservador con observación
hospitalaria.
Todos los demás casos requieren drenaje con tubo pleural. Si el NE es secundario, el calibre del
tubo debe tener un tamaño igual o superior a 24 Fr; si el NE es primario pequeño, de 8 a 10 Fr, y si es
primario grande (A – B ≥ 2 cm), el calibre debe ser igual o superior a 18 Fr. La descripción de la
técnica, sus indicaciones y contraindicaciones se tratan en el capítulo 191.
El neumotórax a tensión se considera una emergencia médica y requiere tratamiento
descompresivo, incluso antes de la confirmación radiológica. Se procede a la colocación, en el
segundo espacio intercostal, por encima del borde costal superior, de un angiocatéter de una longitud
superior a 4,5 cm, conectado a una jeringa con anestesia local o suero estéril (v. caps. 164 y 191). Si se
obtiene un burbujeo fácil de aire se extrae la aguja metálica y se deja colocado el catéter de plástico
dentro del tórax hasta el tratamiento definitivo, que consiste en la inserción de un tubo pleural (calibre
≥ 24 Fr) en alguno de los puntos torácicos de punción (figs. 42.2 y 42.3).
En el hemoneumotórax espontáneo se coloca igualmente un tubo pleural (calibre ≥ 24 Fr) si no
existe indicación quirúrgica de entrada. Se monitoriza la permeabilidad y el débito por el drenaje. Si
éste es superior a 700 ml durante la primera hora, o superior a 200 ml/h, durante 2 h consecutivas, se
indica cirugía de urgencia.
Figura 42.2 Material necesario para la colocación de un catéter pleural y un tubo pleural. Sistema de sello de agua.
Figura 42.3 Localizaciones de punción y colocación del tubo de tórax en un neumotórax. A) Visión lateral. B) Visión
anteroposterior.
Bibliografía recomendada
Currie GP, Alluri R, Christie GL, Legge JS. Pneumothorax: an update. Postgrad Med J. 2007;83:461-465.
Henry M, Arnold T, Harvey J. Pleural Diseases Group, Standards of Care Committee, British Thoracic Society. BTS guidelines for the
management of spontaneous pneumothorax. Thorax. 2003;58:ii39-ii52.
Kosowsky JM. Pleural disease. In: Marx JA, Hockberger RS, Wall RM, editors. Rosen’s Emergency Medicine. Concepts and clinical
practice. 6.ª ed. Filadelfia: Mosby Elsevier; 2006:1143-1154.
Kuester JR, Frese S, Stein RM, Roth T, Beshay M, Schmid RA. Treatment of primary spontaneous pneumothorax in Switzerland:
results a survey. Interact Cardiovasc and Thorac Surg. 2006;5:139-144.
Laws D, Neville E, Duffy J, on behalf of the British Thoracic Society Pleural Disease Group. BTS guidelines for the insertion of a
chest drain. Thorax. 2003;58:ii53-ii59.
Wakai A, O’Sullivan RG, McCabe G. Aspiración simple versus drenaje con tubo intercostal para el neumotórax espontáneo primario
en adultos (Revisión Cochrane traducida). In La Biblioteca Cochrane Plus. Oxford, UK: John Ltd; 2008. Número 2.: Disponible
en: http://www.update-software.com. (Traducida de The Cochrane Library, 2008. Chichester, UK: John Wiley & Sons, Ltd.)
Young WFJr, Humphries RL. Spontaneous and iatrogenic pneumothorax. In: Tintinalli JE, Kelen GD, Stapczynski JS, editors.
Emergency medicine. A comprehensive study guide. 6.ª ed. Nueva York: McGraw Hill; 2004:462-464.
Zehtabchi S, Rios C. Management of emergency departament patients with primary spontaneous pneumothorax: needle aspiration o
tube thoracostomy. Ann Emerg Med. 2008;51:91-101.